大规模应用SARS-CoV-2疫苗是在全球范围内减少SARS-CoV-2传播和预防COVID-19症状的主要途径。SARS-CoV-2灭活疫苗是许多国家使用最广泛的疫苗类型之一。然而,临床试验数据表明:SARS-CoV-2灭活疫苗对COVID-19感染者(不含无症状感染者)的保护率为65%-85%,15%-35%人群在两剂免疫后仍未受到充分保护1-4。依据接种后人体SARS-CoV-2特异性中和抗体水平,将两剂免疫程序后仍未获得免疫保护或获得的免疫保护不充分人群称之为“无应答者”。促使无应答者获取免疫保护对于通过大规模疫苗接种建立的群体免疫屏障至关重要。第三剂灭活疫苗已被证明在一般人群中可将中和抗体反应提高3-5倍5,且许多国家正在启动大规模应用第三剂作为“加强剂”剂量,但其是否能诱导无反应者产生足够抗体水平的能力尚不清楚。
2022年4月15日,云南大学生物资源保护与利用国家重点实验室张子杰团队和云南大学附属医院(云南省第二人民医院)中心实验室、感染科韦嘉团队在National Science Review(IF=17.2)杂志上发表了题为A third dose of inactivated SARS-CoV-2 vaccine induces robust antibody responses in people with inadequate response to two-dose vaccination的文章,张子杰研究员、韦嘉教授和周太成副研究员为本文的通讯作者,石田培博士研究生、李敖硕士研究生等为该文章的共同第一作者。该研究首次基于国内大群体报道了在完成两剂免疫标准程序后,约4.9%人群不能诱导出可检测的抗体水平,约20%人群抗体水平临床保护率较低。本研究数据显示99%无(弱)应答者在接种第三剂加强疫苗后实现中和抗体血清学转化,但第三剂疫苗在无应答者中诱导的免疫对于变异株的保护有所降低。
研究团队此前已在新冠疫苗响应个体差异方面进行了一系列的探索,此项研究是在之前的基础上更进一步的探索。该研究从4,565名志愿者中入组符合条件的志愿者进行血清学检测(包括新冠特异性中和抗体、免疫球蛋白G(IgG)和免疫球蛋白M(IgM))。抗体检测结果表明4.9% 的志愿者(105名)在完成两剂疫苗接种两周后未能检测到中和抗体(Figure 1)。IgG的分布与中和抗体相似,而IgM的血清转化率较低。接种第三针后,前两剂无应答者获得了更高的抗体水平:104名无应答者(99%)的中和抗体水平通过了血清阳性临界值,几何平均滴度为19,比两剂后抗体水平提高12倍(P=4.6×10-49),比普通人群两剂后抗体几何平均滴度高1.8倍(P=6.7×10-9),比COVID-19恢复期患者的几何平均滴度高1.4倍(P=6.2×10-4)。此外,研究中也提到第三剂疫苗后所获得抗体增量与受试性别、年龄、BMI、身体健康状况、第二次和第三次接种间的时间间隔等因素的相关性,分析结果提示性别、年龄、BMI、身体健康状况因素并不能解释中和抗体水平增加的变化。
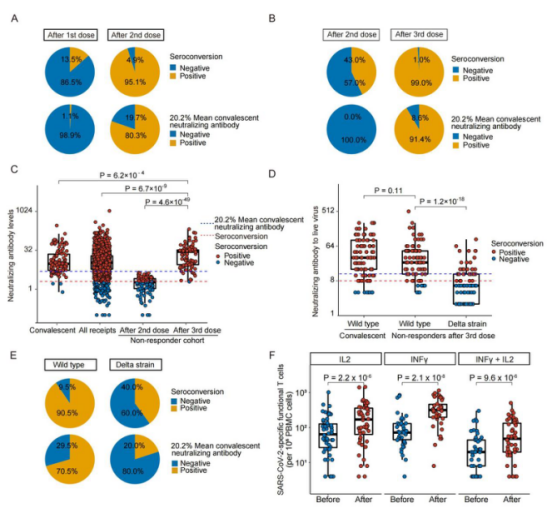
图1 无应答人群接种第三剂灭活疫苗免疫应答
由于群体中和抗体滴度均由磁微粒化学发光法测算,作者通过增设活病毒中和试验进一步验证针对SARS-CoV-2原始毒株和Delta变异毒株的个体中和水平。结果指出SARS-CoV-2原始毒株病毒中和试验血清阳性率为90.5%,与磁微粒化学发光法中和水平高度相关(皮尔逊相关系数=0.84),证实大多数无反应者在第三次接种后可获得对野生型SARS-CoV-2的免疫保护。然而,SARS-CoV-2 Delta变异毒株病毒中和试验血清阳性率只有为40%,与野生型病毒相比,中和活性显著降低(P=1.2×10-18)。抗体数据表明,第三剂SARS-CoV-2灭活疫苗是对两剂疫苗免疫响应不足的人获得体液免疫保护的有效策略,但面对Delta变异毒株,由第三剂灭活疫苗在无(弱)应答人群中诱导的免疫保护较为有限。
此外,该研究对无应答者三针后的细胞免疫反应进行了分析。通过荧光免疫斑点(FluoroSpot)试验和活化诱导标记物(AIM)试验检测T细胞对SARS-CoV-2的效应。FluoroSpot结果表明,在SARS-CoV-2肽库刺激下,大多数无应答志愿在第三剂接种前后均检测到了SARS-cov-2特异性T细胞,接种后与接种前相比,T细胞计数总体增加(Figure 1),表明第三剂接种可促进Th1细胞的反应。AIM与FluoroSpot试验结果一致,87.5%和45%的志愿者对SARS-CoV-2肽库分别有CD4+和CD8+ T细胞反应。这证实了尽管体液免疫响应较差,但大多数无应答者在第三剂接种前已经获得了针对SARS-CoV-2的CD4+ T细胞免疫力。
除免疫原性外,作者也讨论了疫苗接种的安全性。在三次接种中,未出现3级或4级不良反应事件。1级或2级不良反应事件中:与前两剂相比,第三剂接种后局部(注射部位)不良反应更加常见,而全身肌肉疼痛和头痛等全身不良反应的频率反而降低。
综上,该研究表明接种第三剂SARS-CoV-2灭活疫苗(加强针)是疫苗无(弱)应答者获得体液免疫保护的有效策略,因此建议全面接种第三剂疫苗,以确保大多数疫苗接种者可获得体液免疫。该研究揭示了群体第三剂疫苗接种对于弥补部分人群应答不良带来的免疫屏障漏洞的重要性和必要性,为当下大规模加强剂疫苗接种计划和疫苗迭代提供重要理论支撑。
原文链接:
https://doi.org/10.1093/nsr/nwac066
参考文献
1. Zhang Y, Zeng G, Pan H, et al. Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine in healthy adults aged 18–59 years: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial. The Lancet Infectious Diseases 2021; 21(2): 181-92.
2. Jara A, Undurraga EA, González C, et al. Effectiveness of an Inactivated SARS-CoV-2 Vaccine in Chile. New England Journal of Medicine 2021.
3. Murat K, Ediz TE. The Effectiveness of Inactivated SARS-CoV-2 Vaccine (CoronaVac) on Antibody Response in Participants Aged 65 Years and Older. J Med Virol 2021.
4. Tanriover MD, Doğanay HL, Akova M, et al. Efficacy and safety of an inactivated whole-virion SARS-CoV-2 vaccine (CoronaVac): interim results of a double-blind, randomised, placebo-controlled, phase 3 trial in Turkey. The Lancet 2021; 398(10296): 213-22.
5. Pan H, Wu Q, Zeng G, et al. Immunogenicity and safety of a third dose, and immune persistence of CoronaVac vaccine in healthy adults aged 18-59 years: interim results from a double-blind, randomized, placebo-controlled phase 2 clinical trial. medRxiv 2021: 2021.07.23.21261026.

